Códon de parada
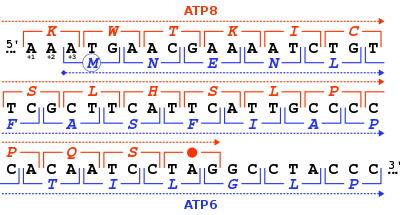
Em biologia molecular (especificamente biossíntese de proteínas), um códon de parada (ou códon de terminação) é um códon (tripleto de nucleotídeos dentro do RNA mensageiro) que sinaliza a terminação do processo de tradução da proteína atual. A maioria dos códons no RNA mensageiro corresponde à adição de um aminoácido a uma cadeia polipeptídica em crescimento, que pode finalmente se tornar uma proteína; os códons de parada sinalizam o término desse processo ligando-se a fatores de liberação, que fazem com que as subunidades ribossômicas se desassociem, liberando a cadeia de aminoácidos.
Embora os códons de início precisem de sequências ou fatores de iniciação próximos para iniciar a tradução, um códon de parada por si só é suficiente para iniciar a terminação.
Propriedades
Códons padrão
No código genético padrão, existem três códons de terminação diferentes:
| Desculpa. | Código padrão (Tabela de tradução) | Nome | ||
|---|---|---|---|---|
| DNA | RNA | |||
TAG | UAG | STOP = Ter (*) | "amber" | |
TAA | UAA | STOP = Ter (*) | "Chre" | |
TGA | UGA | STOP = Ter (*) | "opal" (ou "umber") | |
Códons de parada alternativos
Existem variações no código genético padrão, e códons de parada alternativos foram encontrados nos genomas mitocondriais de vertebrados, Scenedesmus obliquus e Thraustochytrium.
| Código genético | Tradução mesa de mesa | Desculpa. | Tradução com este código | Tradução padrão | ||||
|---|---|---|---|---|---|---|---|---|
| DNA | RNA | |||||||
| Vertebrado mitocondrial | 2 | AGA | AGA | STOP = Ter (*) | Arg (R) | |||
AGG | AGG | STOP = Ter (*) | Arg (R) | |||||
| Cenasmus obliquus mitocondrial | 22 | TCA | UCA | STOP = Ter (*) | Ser (S) | |||
| mitocondrial de Thraustochytrium | 23 | TTA | UUA | STOP = Ter (*) | Leu (L) | |||
| Propriedades bioquímicas aminado-ácido | Não poluente | Polar | Básico | Ácido | Terminação: stop codon |
Códons de parada reatribuídos
O código genético nuclear é flexível, conforme ilustrado por códigos genéticos variantes que reatribuem códons de parada padrão aos aminoácidos.
| Código genético | Tradução mesa de mesa | Desculpa. | Condicionado tradução | Tradução padrão | ||||
|---|---|---|---|---|---|---|---|---|
| DNA | RNA | |||||||
| Nuclear de Karyorelict | 27 | TGA | UGA | Ter (*) | ou | Trp (W) | Ter (*) | |
| nuclear de Condylostoma | 28 | TAA | UAA | Ter (*) | ou | Gln (Q) | Ter (*) | |
TAG | UAG | Ter (*) | ou | Gln (Q) | Ter (*) | |||
TGA | UGA | Ter (*) | ou | Trp (W) | Ter (*) | |||
| Nuclear de explosão | 31 | TAA | UAA | Ter (*) | ou | Glu (E) | Ter (*) | |
TAG | UAG | Ter (*) | ou | Glu (E) | Ter (*) | |||
Tradução
Em 1986, foram fornecidas evidências convincentes de que a selenocisteína (Sec) foi incorporada co-traducionalmente. Além disso, o códon que direciona parcialmente sua incorporação na cadeia polipeptídica foi identificado como UGA, também conhecido como códon de terminação opala. Diferentes mecanismos para substituir a função de terminação deste códon foram identificados em procariontes e em eucariotos. Uma diferença particular entre estes reinos é que os elementos cis parecem restritos à vizinhança do códon UAG nos procariontes, enquanto nos eucariotos esta restrição não está presente. Em vez disso, esses locais parecem desfavorecidos, embora não proibidos.
Em 2003, um artigo histórico descreveu a identificação de todas as selenoproteínas conhecidas em humanos: 25 no total. Análises semelhantes foram realizadas para outros organismos.
O códon UAG pode ser traduzido em pirrolisina (Pyl) de maneira semelhante.
Distribuição genômica
A distribuição de códons de parada no genoma de um organismo não é aleatória e pode se correlacionar com o conteúdo de GC. Por exemplo, o E. coli K-12 contém 2.705 TAA (63%), 1.257 TGA (29%) e 326 TAG (8%) códons de parada (conteúdo de GC 50,8%). Além disso, os substratos para o fator de liberação 1 dos códons de parada ou fator de liberação 2 estão fortemente correlacionados com a abundância de códons de parada. O estudo em larga escala de bactérias com uma ampla gama de conteúdos de GC mostra que, embora a frequência de ocorrência de TAA esteja negativamente correlacionada com o conteúdo de GC e a frequência de ocorrência de TGA esteja positivamente correlacionada com o conteúdo de GC, a frequência de ocorrência do códon de parada TAG, que geralmente é o códon de parada minimamente usado em um genoma, não é influenciado pelo conteúdo de GC.
Reconhecimento
O reconhecimento de códons de parada em bactérias tem sido associado ao chamado 'anticódon tripeptídeo', um motivo de aminoácido altamente conservado em RF1 (PxT) e RF2 (SPF). Embora isto seja apoiado por estudos estruturais, foi demonstrado que a hipótese do anticódon tripeptídico é uma simplificação excessiva.
Nomenclatura
Os códons de parada receberam historicamente muitos nomes diferentes, pois cada um deles correspondia a uma classe distinta de mutantes que se comportavam de maneira semelhante. Esses mutantes foram isolados pela primeira vez em bacteriófagos (T4 e lambda), vírus que infectam a bactéria Escherichia coli. Mutações em genes virais enfraqueceram sua capacidade infecciosa, às vezes criando vírus que foram capazes de infectar e crescer apenas em certas variedades de E. coli.
Mutações âmbar (UAG)
Elas foram o primeiro conjunto de mutações sem sentido a serem descobertas, isoladas por Richard H. Epstein e Charles Steinberg e batizadas em homenagem a seu amigo e estudante graduado da Caltech Harris Bernstein, cujo sobrenome significa "âmbar" em alemão (cf. Bernstein).
Os vírus com mutações âmbar são caracterizados pela capacidade de infectar apenas certas cepas de bactérias, conhecidas como supressores âmbar. Essas bactérias carregam sua própria mutação que permite a recuperação da função dos vírus mutantes. Por exemplo, uma mutação no tRNA que reconhece o códon de parada âmbar permite que a tradução seja "lida" o códon e produzir uma proteína completa, recuperando assim a forma normal da proteína e "suprimindo" a mutação âmbar. Assim, os mutantes âmbar são uma classe inteira de mutantes de vírus que podem crescer em bactérias que contêm mutações supressoras de âmbar. Supressores semelhantes também são conhecidos para códons de parada ocre e opala.
Moléculas de tRNA que transportam aminoácidos não naturais foram projetadas para reconhecer o códon de parada âmbar no RNA bacteriano. Esta tecnologia permite a incorporação de aminoácidos ortogonais (como a p-azidofenilalanina) em locais específicos da proteína alvo.
Mutações ocre (UAA)
Foi a segunda mutação do códon de parada a ser descoberta. Remanescente da habitual cor amarelo-laranja-marrom associada ao âmbar, este segundo códon de parada recebeu o nome de "ochre", um pigmento mineral laranja-marrom-avermelhado.
Os vírus mutantes ocre tinham uma propriedade semelhante aos mutantes âmbar, pois recuperavam a capacidade infecciosa em certas cepas supressoras de bactérias. O conjunto de supressores ocres era distinto dos supressores âmbar, de modo que os mutantes ocres foram inferidos como correspondendo a um trio de nucleotídeos diferente. Através de uma série de experimentos de mutação comparando esses mutantes entre si e com outros códons de aminoácidos conhecidos, Sydney Brenner concluiu que as mutações âmbar e ocre correspondiam aos trigêmeos de nucleotídeos "UAG" e "UAA".
Mutações opala ou umber (UGA)
O terceiro e último códon de parada no código genético padrão foi descoberto logo depois e corresponde ao trio de nucleotídeos "UGA".
Para continuar combinando com o tema dos minerais coloridos, o terceiro códon sem sentido passou a ser conhecido como "opal", que é um tipo de sílica que apresenta uma variedade de cores. Mutações sem sentido que criaram esse códon de parada prematuro foram mais tarde chamadas de mutações opala ou mutações umber.
Mutações e doenças
Bobagem
Mutações sem sentido são alterações na sequência de DNA que introduzem um códon de parada prematuro, fazendo com que qualquer proteína resultante seja anormalmente encurtada. Isto muitas vezes causa uma perda de função na proteína, uma vez que partes críticas da cadeia de aminoácidos não estão mais montadas. Devido a esta terminologia, os códons de parada também são chamados de códons sem sentido.
Sem parar
Uma mutação contínua, também chamada de variante stop-loss, é uma mutação pontual que ocorre dentro de um códon de parada. Mutações ininterruptas causam a tradução contínua de uma cadeia de mRNA no que deveria ser uma região não traduzida. A maioria dos polipeptídeos resultantes de um gene com mutação contínua perdem sua função devido ao seu comprimento extremo e ao impacto no dobramento normal. As mutações contínuas diferem das mutações sem sentido porque não criam um códon de parada, mas, em vez disso, excluem um. As mutações contínuas também diferem das mutações missense, que são mutações pontuais em que um único nucleotídeo é alterado para causar a substituição por um aminoácido diferente. Mutações contínuas têm sido associadas a muitas doenças hereditárias, incluindo distúrbios endócrinos, doenças oculares e distúrbios do desenvolvimento neurológico.
Paradas ocultas
Paradas ocultas são códons contínuos que seriam lidos como códons de parada se fossem deslocados em +1 ou -1. Estes terminam prematuramente a tradução se a mudança de quadro correspondente (como devido a um deslizamento de RNA ribossômico) ocorrer antes da parada oculta. A hipótese é que isso diminua o desperdício de recursos em proteínas não funcionais e a produção de potenciais citotoxinas. Pesquisadores da Louisiana State University propõem a hipótese da emboscada, para a qual são selecionadas paradas ocultas. Os códons que podem formar paradas ocultas são usados nos genomas com mais frequência em comparação com os códons sinônimos que, de outra forma, codificariam o mesmo aminoácido. O rRNA instável em um organismo se correlaciona com uma frequência mais alta de paradas ocultas. No entanto, esta hipótese não pôde ser validada com um conjunto de dados maior.
Códons de parada e paradas ocultas juntos são chamados coletivamente de sinais de parada. Pesquisadores da Universidade de Memphis descobriram que as proporções dos sinais de parada nos três quadros de leitura de um genoma (referido como razão de sinais de parada de tradução ou TSSR) de bactérias geneticamente relacionadas, apesar de suas grandes diferenças no conteúdo do gene, são muito semelhantes.. Este valor genômico-TSSR quase idêntico de bactérias geneticamente relacionadas pode sugerir que a expansão do genoma bacteriano é limitada pelo viés único dos sinais de parada daquela espécie bacteriana.
Leitura da tradução
A supressão do códon de parada ou leitura translacional ocorre quando na tradução um códon de parada é interpretado como um códon de sentido, ou seja, quando um aminoácido (padrão) é &# 39;codificado' pelo códon de parada. Os tRNAs mutados podem ser a causa da leitura, mas também de certos motivos nucleotídicos próximos ao códon de parada. A leitura translacional é muito comum em vírus e bactérias e também foi encontrada como um princípio regulador de genes em humanos, leveduras, bactérias e drosófilas. Este tipo de leitura translacional endógena constitui uma variação do código genético, porque um códon de parada codifica um aminoácido. No caso da malato desidrogenase humana, o codão de terminação é lido com uma frequência de cerca de 4%. O aminoácido inserido no códon de parada depende da identidade do próprio códon de parada: Gln, Tyr e Lys foram encontrados para os códons UAA e UAG, enquanto Cys, Trp e Arg para o códon UGA foram identificados por massa espectrometria. A extensão da leitura em mamíferos tem extensões amplamente variáveis e pode diversificar amplamente o proteoma e afetar a progressão do câncer.
Usar como marca d’água
Em 2010, quando Craig Venter revelou a primeira célula de reprodução totalmente funcional controlada por DNA sintético, ele descreveu como sua equipe usou códons de parada frequentes para criar marcas d'água em RNA e DNA para ajudar a confirmar se os resultados eram realmente sintéticos (e não contaminados ou caso contrário), usando-o para codificar os autores. nomes e endereços de sites.
Contenido relacionado
Alexandre Fleming
Emil Theodor Kocher
Kary Mullis
Lactase
Konrad Lorenz