Clorina
Na química orgânica, clorinas são pigmentos tetrapirarrolos que são porfirinas parcialmente hidrogenadas. O clorina pai é um composto instável que sofre oxidação do ar em porfina. O nome clorina deriva da clorofila. As clorofilas são clorinas contendo magnésio e ocorrem como pigmentos fotossintéticos em cloroplastos. O termo "clorin " Estritamente falando refere -se a apenas compostos com o mesmo estado de oxidação do anel que a clorofila.
Clorinas são excelentes agentes de fotossensibilização. Vários análogos de clorinas sintéticas, como m-tetra-hidroxifenilclorina (MTHPC) e clorina mono-l-aspartil E6, são efetivamente empregados em terapia fotodinâmica experimental como fotossensibilizadores.
Clorofilas
O clorina mais abundante é a clorofila de pigmento fotossintético. As clorofilas têm um quinto anel contendo cetona, diferente das clorinas. Existe diversas clorofilas, como clorofila A, clorofila B, clorofila D, clorofila e , clorofila f e clorofila g . As clorofilas geralmente apresentam magnésio como um átomo de metal central, substituindo os dois centros N H no pai.
Variação
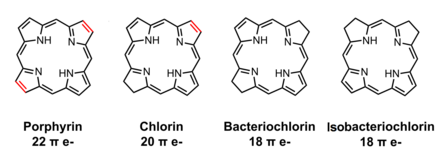
micróbios produzem duas variantes reduzidas de clorina, bacterioclorinas e isobacterioclorinas. As bacterioclorinas são encontradas em algumas bacterioclorofilas; A estrutura do anel é produzida pela clorofilida a redutase (COR), reduzindo um anel de clorina no boud duplo C7-8. As isobacterioclorinas são encontradas na natureza principalmente como siro -hidroclorina, um intermediário biossintético de vitamina B12, produzido sem passar por um clorina. Nos organismos vivos, ambos são derivados do uroporfirinogênio III, um intermediário quase universais na biossíntese de tetrapirrol.
Cloretos sintéticos
numerosas clorinas sintéticas com diferentes grupos funcionais e/ou modificações de anel foram examinadas.
Clorinas contratadas podem ser sintetizadas pela redução da subporfirina B (III) ou pela oxidação da subclorina B (III) correspondente. As subclorinas B (iii) foram sintetizadas diretamente como subclorina meso -ster B (iii) de meso-mester tripyromethane, essa classe de composto mostrou um rendimento quântico e singlet de fluorescência muito bom Eficiência de produção de oxigênio
Ver também
- Corrimão
- Terapia fotográfica
Leitura adicional
- Juse ́lius, Jonas; Sundholm, Dage (2000). «The aromatic pathways of porphins, chlorins and bacteriochlorins» (em inglês). Química Física Física. 2 (10): 2145–2151. Bibcode:2000PCCP....2.2145J. doi:10.1039/b000260g.
Referências
- ^ Gerard P. Moss (1988). "Nomenclatura de Tetrapyrroles. Recomendações 1986". Revista Europeia de Bioquímica. 178 (2): 277–328.10.1111/j.1432-1033.1988.tb14453.x. PMID 3208761.
- ^ Battersby, Alan R. (2000). «Tetrapyrroles: The pigments of life» (em inglês). Relatórios de produtos naturais. 17. (6): 507–526. doi:10.1039/b002635m. PMID 11152419.
- ^ Spikes, John D. (julho de 1990). «New trend in photobiology» (em inglês). Journal of Photochemistry and Photobiology B: Biologia. 6 (3): 259–274. doi:10.1016/1011-1344(90)85096-F. PMID 2120404.
- ^ K. Eszter, Borbas. Manual de Porfirina Ciência: 181: Clorins. worldscientific. doi:10.1142/9789813149564_0001. ISBN 9814322326.
- ^ Chew, Aline Gomez Maqueo; Bryant, Donald A. (2007). «Chlorophyll Biosynthesis in Bacteria: The Origins of Structural and Functional Diversity» (em inglês). Revisão Anual de Microbiologia. 61: 113–129. doi:10.1146/annurev.micro.61.080706.093242. PMID 17506685.
- ^ Battersby, Alan R. (2000). «Tetrapyrroles: The pigments of life: A Millennium review» (em inglês). Relatórios de produtos naturais. 17. (6): 507–526. doi:10.1039/B002635M. PMID 11152419.
- ^ Taniguchi, Masahiko; Lindsey, Jonathan S. (2017). «Synthetic Chlorins, Possible Surrogates for Chlorophylls, Prepared by Derivatization of Porphyrins» (em inglês). Comentários de produtos químicos. 117 (2): 344-535. doi:10.1021/acs.chemrev.5b00696. OSTI 1534468. PMID 27498781.
- ^ Osuka, Atsuhiro; Kim, Dongho (2008). «Synthesis and Characterization of meso-Aryl-Substituted Subchlorins» (em inglês). Journal of the American Chemical Society. 130 (2): 438–439. doi:10.1021/ja078042b. PMID 18095693.
- ^ Chandra, Brijesh; Soman, Rahul; Sathish Kumar, B.; Jose, K. V. Jovan; Panda, Pradeepta K. (3 Dec 2020). "Meso-Free Boron(III)subchlorin and Its μ-Oxo Dimer with Interacting Chromophores". Letras orgânicas. 22 (24): 9735–9739. doi:10.1021/acs.orglett.0c03813. PMID 33270460. S2CID 227282229.
- ^ Somã, Rahul; Chandra, Brijesh; Bhat, Ishfaq A.; Kumar, B. Sathish; Hossain, Sk Saddam; Nandy, Sridatri; Jose, K. V. Jovan; Panda, Pradeepta K. (15 Jul 2021). «A2B- and A3-Type Boron(III)Subchlorins Derived from meso-Diethoxycarbonyltripyrrane: Synthesis and Photophysical Exploration» (em inglês). O Jornal de Química Orgânica. 86 (15): 10280–10287. doi:10.1021/acs.joc.1c01001. PMID 34264670. S2CID 235959639.