Anfetamina
A anfetamina (contraída da alfa-metilfenetilamina) é um forte estimulante do sistema nervoso central (SNC) usado no tratamento do transtorno de déficit de atenção e hiperatividade (TDAH), narcolepsia e obesidade. Também é comumente usado como uma droga recreativa. A anfetamina foi descoberta em 1887 e existe como dois enantiômeros: levoanfetamina e dextroanfetamina. Anfetamina refere-se apropriadamente a um produto químico específico, a base livre racêmica, que é partes iguais dos dois enantiômeros em suas formas de amina pura. O termo é freqüentemente usado informalmente para se referir a qualquer combinação dos enantiômeros, ou a qualquer um deles sozinho. Historicamente, tem sido usado para tratar congestão nasal e depressão. A anfetamina também é usada como um intensificador de desempenho atlético e cognitivo, e recreacionalmente como afrodisíaco e eufórico. É um medicamento prescrito em muitos países, e a posse e distribuição não autorizadas de anfetaminas são frequentemente controladas devido aos riscos significativos à saúde associados ao uso recreativo.
A primeira anfetamina farmacêutica foi Benzedrine, uma marca usada para tratar uma variedade de condições. Atualmente, a anfetamina farmacêutica é prescrita como anfetamina racêmica, Adderall, dextroanfetamina ou o pró-fármaco inativo lisdexanfetamina. A anfetamina aumenta a monoamina e a neurotransmissão excitatória no cérebro, com seus efeitos mais pronunciados direcionados aos sistemas de neurotransmissores de norepinefrina e dopamina.
Em doses terapêuticas, a anfetamina causa efeitos emocionais e cognitivos, como euforia, mudança no desejo sexual, aumento da vigília e melhora do controle cognitivo. Induz efeitos físicos, como melhor tempo de reação, resistência à fadiga e aumento da força muscular. Doses maiores de anfetamina podem prejudicar a função cognitiva e induzir rápida degradação muscular. O vício é um risco sério com o uso recreativo pesado de anfetaminas, mas é improvável que ocorra com o uso médico de longo prazo em doses terapêuticas. Doses muito altas podem resultar em psicose (por exemplo, delírios e paranóia), que raramente ocorre em doses terapêuticas, mesmo durante o uso prolongado. As doses recreativas são geralmente muito maiores do que as doses terapêuticas prescritas e apresentam um risco muito maior de efeitos colaterais graves.
A anfetamina pertence à classe das fenetilaminas. É também o composto parental de sua própria classe estrutural, as anfetaminas substituídas, que incluem substâncias proeminentes como bupropiona, catinona, MDMA e metanfetamina. Como membro da classe da fenetilamina, a anfetamina também está quimicamente relacionada aos neuromoduladores de aminas de ocorrência natural, especificamente a fenetilamina e a N-metilfenetilamina, ambas produzidas no corpo humano. A fenetilamina é o composto parental da anfetamina, enquanto a N-metilfenetilamina é um isômero posicional da anfetamina que difere apenas na colocação do grupo metil.
Usos
Médico
A anfetamina é usada para tratar o transtorno de déficit de atenção e hiperatividade (TDAH), narcolepsia (um distúrbio do sono) e obesidade, e às vezes é prescrita off-label por suas indicações médicas anteriores, particularmente para depressão e dor crônica. Sabe-se que a exposição prolongada a anfetaminas em doses suficientemente altas em algumas espécies animais produz desenvolvimento anormal do sistema de dopamina ou danos nos nervos, mas em alguns casos em humanos com TDAH, as anfetaminas farmacêuticas em dosagens terapêuticas podem melhorar o desenvolvimento do cérebro e o crescimento dos nervos. Revisões de estudos de ressonância magnética (MRI) sugerem que o tratamento a longo prazo com anfetamina diminui as anormalidades na estrutura e função cerebral encontradas em indivíduos com TDAH e melhora a função em várias partes do cérebro, como o núcleo caudado direito dos gânglios da base.
Revisões de pesquisas clínicas sobre estimulantes estabeleceram a segurança e a eficácia do uso contínuo de anfetaminas a longo prazo para o tratamento do TDAH. Ensaios clínicos randomizados de terapia estimulante contínua para o tratamento de TDAH por 2 anos demonstraram eficácia e segurança do tratamento. Duas revisões indicaram que a terapia estimulante contínua de longo prazo para o TDAH é eficaz para reduzir os sintomas centrais do TDAH (ou seja, hiperatividade, desatenção e impulsividade), melhorando a qualidade de vida e o desempenho acadêmico e produzindo melhorias em um grande número de aspectos funcionais. resultados em 9 categorias de resultados relacionados a acadêmicos, comportamento antissocial, direção, uso de drogas não medicinais, obesidade, ocupação, autoestima, uso de serviços (ou seja, serviços acadêmicos, ocupacionais, de saúde, financeiros e jurídicos) e função social. Uma revisão destacou um estudo randomizado controlado de nove meses de tratamento com anfetamina para TDAH em crianças que encontrou um aumento médio de 4,5 pontos de QI, aumentos contínuos na atenção e reduções contínuas em comportamentos disruptivos e hiperatividade. Outra revisão indicou que, com base nos estudos de acompanhamento mais longos realizados até o momento, a terapia estimulante vitalícia que começa durante a infância é continuamente eficaz para controlar os sintomas do TDAH e reduz o risco de desenvolver um transtorno por uso de substâncias quando adulto.
Modelos atuais de TDAH sugerem que ele está associado a deficiências funcionais em alguns dos sistemas de neurotransmissores do cérebro; essas deficiências funcionais envolvem neurotransmissão de dopamina prejudicada na projeção mesocorticolímbica e neurotransmissão de norepinefrina nas projeções noradrenérgicas do locus coeruleus para o córtex pré-frontal. Psicoestimulantes como metilfenidato e anfetamina são eficazes no tratamento do TDAH porque aumentam a atividade dos neurotransmissores nesses sistemas. Aproximadamente 80% das pessoas que usam esses estimulantes observam melhorias nos sintomas do TDAH. Crianças com TDAH que usam medicamentos estimulantes geralmente têm melhores relacionamentos com colegas e familiares, têm melhor desempenho na escola, são menos distraídas e impulsivas e têm períodos de atenção mais longos. As revisões Cochrane sobre o tratamento de TDAH em crianças, adolescentes e adultos com anfetaminas farmacêuticas afirmaram que estudos de curto prazo demonstraram que essas drogas diminuem a gravidade dos sintomas, mas apresentam taxas de descontinuação mais altas do que medicamentos não estimulantes devido a seus efeitos adversos efeitos colaterais. Uma revisão da Cochrane sobre o tratamento do TDAH em crianças com transtornos de tiques, como a síndrome de Tourette, indicou que os estimulantes em geral não pioram os tiques, mas altas doses de dextroanfetamina podem exacerbar os tiques em alguns indivíduos.
Melhorando o desempenho
Desempenho cognitivo
Em 2015, uma revisão sistemática e uma meta-análise de ensaios clínicos de alta qualidade descobriram que, quando usada em doses baixas (terapêuticas), a anfetamina produz melhorias modestas, mas inequívocas, na cognição, incluindo memória de trabalho, memória episódica de longo prazo, controle inibitório e alguns aspectos da atenção em adultos saudáveis normais; sabe-se que esses efeitos de aumento da cognição da anfetamina são parcialmente mediados pela ativação indireta do receptor de dopamina D1 e do adrenoceptor α2 no córtex pré-frontal. Uma revisão sistemática de 2014 descobriu que baixas doses de anfetamina também melhoram a consolidação da memória, levando a uma melhor recuperação de informações. Doses terapêuticas de anfetamina também aumentam a eficiência da rede cortical, um efeito que medeia melhorias na memória de trabalho em todos os indivíduos. A anfetamina e outros estimulantes do TDAH também melhoram a saliência da tarefa (motivação para realizar uma tarefa) e aumentam a excitação (vigília), promovendo, por sua vez, um comportamento direcionado a um objetivo. Estimulantes como a anfetamina podem melhorar o desempenho em tarefas difíceis e tediosas e são usados por alguns alunos como um auxílio para estudo e realização de testes. Com base em estudos de auto-relato de uso de estimulantes ilícitos, 5–35% dos estudantes universitários usam estimulantes desviados do TDAH, que são usados principalmente para melhorar o desempenho acadêmico, e não como drogas recreativas. No entanto, altas doses de anfetaminas acima da faixa terapêutica podem interferir na memória de trabalho e em outros aspectos do controle cognitivo.
Desempenho físico
A anfetamina é usada por alguns atletas por seus efeitos psicológicos e de melhoria do desempenho atlético, como aumento da resistência e do estado de alerta; no entanto, o uso não medicinal de anfetaminas é proibido em eventos esportivos regulamentados por agências antidoping colegiadas, nacionais e internacionais. Em pessoas saudáveis em doses terapêuticas orais, a anfetamina demonstrou aumentar a força muscular, a aceleração, o desempenho atlético em condições anaeróbicas e a resistência (ou seja, retarda o início da fadiga), ao mesmo tempo em que melhora o tempo de reação. A anfetamina melhora a resistência e o tempo de reação principalmente por meio da inibição da recaptação e liberação de dopamina no sistema nervoso central. A anfetamina e outras drogas dopaminérgicas também aumentam a produção de energia em níveis fixos de esforço percebido, substituindo um "interruptor de segurança", permitindo que o limite de temperatura central aumente para acessar uma capacidade de reserva que normalmente está fora dos limites. Em doses terapêuticas, os efeitos adversos da anfetamina não impedem o desempenho atlético; no entanto, em doses muito mais altas, a anfetamina pode induzir efeitos que prejudicam gravemente o desempenho, como rápida degradação muscular e elevação da temperatura corporal.
Contra-indicações
De acordo com o Programa Internacional de Segurança Química (IPCS) e a Administração de Alimentos e Medicamentos dos Estados Unidos (USFDA), a anfetamina é contraindicada em pessoas com histórico de abuso de drogas, doença cardiovascular, agitação intensa ou ansiedade intensa. Também é contra-indicado em indivíduos com arteriosclerose avançada (endurecimento das artérias), glaucoma (aumento da pressão ocular), hipertireoidismo (produção excessiva de hormônio tireoidiano) ou hipertensão moderada a grave. Essas agências indicam que as pessoas que tiveram reações alérgicas a outros estimulantes ou que estão tomando inibidores da monoamina oxidase (MAOIs) não devem tomar anfetaminas, embora o uso concomitante seguro de anfetaminas e inibidores da monoamina oxidase tenha sido documentado. Essas agências também afirmam que qualquer pessoa com anorexia nervosa, transtorno bipolar, depressão, hipertensão, problemas hepáticos ou renais, mania, psicose, fenômeno de Raynaud, convulsões, problemas de tireóide, tiques ou síndrome de Tourette deve monitorar seus sintomas enquanto estiver tomando anfetamina.. Evidências de estudos em humanos indicam que o uso terapêutico de anfetaminas não causa anormalidades no desenvolvimento do feto ou recém-nascidos (ou seja, não é um teratógeno humano), mas o abuso de anfetaminas representa riscos para o feto. Também foi demonstrado que a anfetamina passa para o leite materno, de modo que o IPCS e o USFDA aconselham as mães a evitar a amamentação ao usá-la. Devido ao potencial para deficiências de crescimento reversíveis, o USFDA aconselha o monitoramento da altura e do peso de crianças e adolescentes prescritos com um fármaco de anfetamina.
Efeitos adversos
Os efeitos colaterais adversos da anfetamina são muitos e variados, e a quantidade de anfetamina usada é o principal fator na determinação da probabilidade e gravidade dos efeitos adversos. Produtos de anfetamina, como Adderall, Dexedrine e seus equivalentes genéricos, são atualmente aprovados pelo USFDA para uso terapêutico de longo prazo. O uso recreativo de anfetaminas geralmente envolve doses muito maiores, que apresentam maior risco de efeitos adversos graves do que as dosagens usadas para fins terapêuticos.
Físico
Os efeitos colaterais cardiovasculares podem incluir hipertensão ou hipotensão de uma resposta vasovagal, fenômeno de Raynaud (redução do fluxo sanguíneo para as mãos e pés) e taquicardia (aumento da frequência cardíaca). Os efeitos colaterais sexuais em homens podem incluir disfunção erétil, ereções frequentes ou ereções prolongadas. Os efeitos colaterais gastrointestinais podem incluir dor abdominal, constipação, diarréia e náusea. Outros possíveis efeitos colaterais físicos incluem perda de apetite, visão turva, boca seca, ranger excessivo dos dentes, sangramento nasal, sudorese profusa, rinite medicamentosa (congestão nasal induzida por drogas), limiar convulsivo reduzido, tiques (um tipo de distúrbio do movimento) e perda de peso. Efeitos colaterais físicos perigosos são raros em doses farmacêuticas típicas.
A anfetamina estimula os centros respiratórios medulares, produzindo respirações mais rápidas e profundas. Em uma pessoa normal em doses terapêuticas, esse efeito geralmente não é perceptível, mas quando a respiração já está comprometida, pode ser evidente. A anfetamina também induz a contração no esfíncter da bexiga urinária, o músculo que controla a micção, o que pode resultar em dificuldade para urinar. Este efeito pode ser útil no tratamento de enurese e perda do controle da bexiga. Os efeitos da anfetamina no trato gastrointestinal são imprevisíveis. Se a atividade intestinal for alta, a anfetamina pode reduzir a motilidade gastrointestinal (a velocidade com que o conteúdo se move pelo sistema digestivo); no entanto, a anfetamina pode aumentar a motilidade quando o músculo liso do trato está relaxado. A anfetamina também tem um leve efeito analgésico e pode aumentar os efeitos analgésicos dos opioides.
Estudos encomendados pelo USFDA de 2011 indicam que em crianças, adultos jovens e adultos não há associação entre eventos cardiovasculares adversos graves (morte súbita, ataque cardíaco e derrame) e o uso médico de anfetaminas ou outros estimulantes do TDAH. No entanto, os produtos farmacêuticos anfetamínicos são contra-indicados em indivíduos com doença cardiovascular.
Psicológico
Em doses terapêuticas normais, os efeitos colaterais psicológicos mais comuns da anfetamina incluem aumento do estado de alerta, apreensão, concentração, iniciativa, autoconfiança e sociabilidade, alterações de humor (humor exaltado seguido de humor levemente deprimido), insônia ou vigília e diminuição sensação de cansaço. Efeitos colaterais menos comuns incluem ansiedade, alteração da libido, grandiosidade, irritabilidade, comportamentos repetitivos ou obsessivos e inquietação; esses efeitos dependem da personalidade do usuário e do estado mental atual. A psicose por anfetaminas (por exemplo, delírios e paranóia) pode ocorrer em usuários pesados. Embora muito rara, esta psicose também pode ocorrer em doses terapêuticas durante terapia de longo prazo. De acordo com o USFDA, "não há evidência sistemática" que os estimulantes produzem comportamento agressivo ou hostilidade.
Também foi demonstrado que a anfetamina produz uma preferência de lugar condicionada em humanos que tomam doses terapêuticas, o que significa que os indivíduos adquirem uma preferência por passar o tempo em locais onde já usaram anfetaminas anteriormente.
Distúrbios de reforço
Vício
Cascata de sinalização no núcleo accumbens que resulta em dependência de anfetamina |
O vício é um risco sério com o uso recreativo pesado de anfetaminas, mas é improvável que ocorra com o uso médico de longo prazo em doses terapêuticas; na verdade, a terapia estimulante vitalícia para TDAH que começa durante a infância reduz o risco de desenvolver transtornos por uso de substâncias quando adulto. A superativação patológica da via mesolímbica, uma via da dopamina que conecta a área tegmental ventral ao núcleo accumbens, desempenha um papel central na dependência de anfetaminas. Indivíduos que frequentemente autoadministram altas doses de anfetaminas têm alto risco de desenvolver dependência de anfetaminas, uma vez que o uso crônico em altas doses aumenta gradativamente o nível de ΔFosB accumbal, um "interruptor molecular" e "proteína de controle mestre" por vício. Uma vez que o ΔFosB do núcleo accumbens é suficientemente superexpresso, ele começa a aumentar a gravidade do comportamento aditivo (isto é, busca compulsiva de drogas) com aumentos adicionais em sua expressão. Embora atualmente não existam drogas eficazes para o tratamento da dependência de anfetaminas, a prática regular de exercícios aeróbicos prolongados parece reduzir o risco de desenvolver tal dependência. A terapia com exercícios melhora os resultados do tratamento clínico e pode ser usada como terapia adjuvante com terapias comportamentais para o vício.
Mecanismos biomoleculares
O uso crônico de anfetaminas em doses excessivas causa alterações na expressão gênica na projeção mesocorticolímbica, que surgem por mecanismos transcricionais e epigenéticos. Os fatores de transcrição mais importantes que produzem essas alterações são Delta FBJ murino osteossarcoma viral oncogene homólogo B (ΔFosB), proteína de ligação do elemento de resposta cAMP (CREB) e nuclear fator-kappa B (NF-κB). ΔFosB é o mecanismo biomolecular mais significativo no vício porque a superexpressão de ΔFosB (ou seja, um nível anormalmente alto de expressão gênica que produz um fenótipo relacionado ao gene pronunciado) nos neurônios espinhosos médios do tipo D1 no núcleo accumbens é necessário e suficiente para muitos dos as adaptações neurais e regula vários efeitos comportamentais (por exemplo, sensibilização de recompensa e autoadministração crescente de drogas) envolvidos no vício. Uma vez que ΔFosB é suficientemente superexpresso, ele induz um estado de dependência que se torna cada vez mais grave com aumentos adicionais na expressão de ΔFosB. Tem sido implicado em vícios de álcool, canabinóides, cocaína, metilfenidato, nicotina, opióides, fenciclidina, propofol e anfetaminas substituídas, entre outros.
ΔJunD, um fator de transcrição, e G9a, uma enzima histona metiltransferase, se opõem à função de ΔFosB e inibem o aumento de sua expressão. A superexpressão suficiente de ΔJunD no núcleo accumbens com vetores virais pode bloquear completamente muitas das alterações neurais e comportamentais observadas no abuso crônico de drogas (ou seja, as alterações mediadas por ΔFosB). Da mesma forma, a hiperexpressão accumbal de G9a resulta em dimetilação acentuadamente aumentada do resíduo de lisina 3 da histona 9 (H3K9me2) e bloqueia a indução da plasticidade neural e comportamental mediada por ΔFosB pelo uso crônico de drogas, que ocorre por meio da repressão mediada por H3K9me2 de fatores de transcrição para ΔFosB e H3K9me2- repressão mediada de vários alvos transcricionais ΔFosB (por exemplo, CDK5). O ΔFosB também desempenha um papel importante na regulação das respostas comportamentais às recompensas naturais, como alimentos saborosos, sexo e exercícios. Uma vez que tanto as recompensas naturais quanto as drogas viciantes induzem a expressão de ΔFosB (ou seja, fazem com que o cérebro produza mais), a aquisição crônica dessas recompensas pode resultar em um estado patológico semelhante de dependência. Consequentemente, ΔFosB é o fator mais significativo envolvido tanto no vício em anfetaminas quanto nos vícios sexuais induzidos por anfetaminas, que são comportamentos sexuais compulsivos resultantes da atividade sexual excessiva e do uso de anfetaminas. Esses vícios sexuais estão associados a uma síndrome de desregulação da dopamina que ocorre em alguns pacientes que tomam drogas dopaminérgicas.
Os efeitos da anfetamina na regulação gênica são dependentes da dose e da via. A maior parte da pesquisa sobre regulação e vício de genes é baseada em estudos com animais com administração intravenosa de anfetaminas em doses muito altas. Os poucos estudos que usaram doses terapêuticas humanas equivalentes (ajustadas ao peso) e administração oral mostram que essas alterações, se ocorrerem, são relativamente menores. Isso sugere que o uso médico de anfetaminas não afeta significativamente a regulação genética.
Tratamentos farmacológicos
Em dezembro de 2019, não havia farmacoterapia eficaz para dependência de anfetaminas. As revisões de 2015 e 2016 indicaram que os agonistas seletivos de TAAR1 têm potencial terapêutico significativo como tratamento para vícios em psicoestimulantes; no entanto, a partir de fevereiro de 2016, os únicos compostos que funcionam como agonistas seletivos de TAAR1 são drogas experimentais. A dependência de anfetaminas é amplamente mediada pela ativação aumentada de receptores de dopamina e receptores NMDA co-localizados no núcleo accumbens; os íons de magnésio inibem os receptores NMDA bloqueando o canal de cálcio do receptor. Uma revisão sugeriu que, com base em testes em animais, o uso de psicoestimulantes patológicos (indutores de dependência) reduz significativamente o nível de magnésio intracelular em todo o cérebro. Foi demonstrado que o tratamento suplementar com magnésio reduz a autoadministração de anfetaminas (ou seja, doses administradas a si mesmo) em humanos, mas não é uma monoterapia eficaz para o vício em anfetaminas.
Uma revisão sistemática e meta-análise de 2019 avaliou a eficácia de 17 farmacoterapias diferentes usadas em ensaios clínicos randomizados (RCTs) para dependência de anfetaminas e metanfetaminas; encontrou apenas evidências de baixa intensidade de que o metilfenidato pode reduzir a autoadministração de anfetaminas ou metanfetaminas. Houve evidência de força baixa a moderada de nenhum benefício para a maioria dos outros medicamentos usados nos ECRs, que incluíam antidepressivos (bupropiona, mirtazapina, sertralina), antipsicóticos (aripiprazol), anticonvulsivantes (topiramato, baclofeno, gabapentina), naltrexona, vareniclina, citicolina, ondansetron, prometa, riluzol, atomoxetina, dextroanfetamina e modafinil.
Tratamentos comportamentais
Uma revisão sistemática de 2018 e meta-análise de rede de 50 estudos envolvendo 12 intervenções psicossociais diferentes para dependência de anfetaminas, metanfetaminas ou cocaína descobriu que a terapia combinada com gerenciamento de contingência e abordagem de reforço comunitário teve a maior eficácia (ou seja, taxa de abstinência) e aceitabilidade (ou seja, menor taxa de abandono). Outras modalidades de tratamento examinadas na análise incluíram monoterapia com gerenciamento de contingência ou abordagem de reforço comunitário, terapia cognitivo-comportamental, programas de 12 etapas, terapias baseadas em recompensa não contingente, terapia psicodinâmica e outras terapias combinadas envolvendo essas modalidades.
Além disso, a pesquisa sobre os efeitos neurobiológicos do exercício físico sugere que o exercício aeróbico diário, especialmente o exercício de resistência (por exemplo, corrida de maratona), previne o desenvolvimento de dependência de drogas e é uma terapia adjuvante eficaz (ou seja, um tratamento suplementar) para anfetamina vício. O exercício leva a melhores resultados de tratamento quando usado como tratamento adjuvante, particularmente para vícios em psicoestimulantes. Em particular, o exercício aeróbico diminui a autoadministração de psicoestimulantes, reduz o restabelecimento (ou seja, recaída) da busca por drogas e induz o aumento da densidade do receptor de dopamina D2 (DRD2) no corpo estriado. Isso é o oposto do uso de estimulantes patológicos, que induz a diminuição da densidade estriatal DRD2. Uma revisão observou que o exercício também pode prevenir o desenvolvimento de um vício em drogas, alterando a imunorreatividade ΔFosB ou c-Fos no corpo estriado ou em outras partes do sistema de recompensa.
| Forma de neuroplasticidade ou plasticidade comportamental | Tipo de reforço | Fontes | |||||
|---|---|---|---|---|---|---|---|
| Opiáceos | Psicoestimulantes | Alimentos de alta gordura ou açúcar | Relações sexuais | Exercício físico (aeróbico) | Enriquecimento ambiental | ||
| expressão ΔFosB em núcleo accumbens D1-tipo MSNs | ↑ | ↑ | ↑ | ↑ | ↑ | ↑ | |
| Plasticidade comportamental | |||||||
| Escalação da ingestão | Sim. | Sim. | Sim. | ||||
| Psicoestimulante sensibilização cruzada | Sim. | Não aplicável | Sim. | Sim. | Atendido | Atendido | |
| Psicoestimulante auto-administração | ↑ | ↑ | ↓ | ↓ | ↓ | ||
| Psicoestimulante preferência de lugar condicionado | ↑ | ↑ | ↓ | ↑ | ↓ | ↑ | |
| Reinstituição do comportamento de busca de drogas | ↑ | ↑ | ↓ | ↓ | |||
| Plasticidade neuroquímica | |||||||
| Fosforilação CREB no núcleo accumbens | ↓ | ↓ | ↓ | ↓ | ↓ | ||
| Resposta de dopamina sensível no núcleo accumbens | Não. | Sim. | Não. | Sim. | |||
| Sinalização da dopamina estrial alterada | ↓DRD2, ↑DRD3 | ↑DRD1, ↓DRD2, ↑DRD3 | ↑DRD1, ↓DRD2, ↑DRD3 | ↑DRD2 | ↑DRD2 | ||
| Sinalização estriatal opióide alterada | Nenhuma mudança ou Receptores ↑μ-opióide | Receptores ↑μ-opióide receptores ↑κ-opióide | Receptores ↑μ-opióide | Receptores ↑μ-opióide | Nenhuma mudança | Nenhuma mudança | |
| Mudanças em peptídeos opióides estriatais | ↑ Dinorphin Nenhuma mudança: enkephalin | ↑ Dinorphin | ↓ | ↑ Dinorphin | ↑ Dinorphin | ||
| Mesocorticolimbic plasticidade sináptica | |||||||
| Número de dendritos no núcleo accumbens | ↓ | ↑ | ↑ | ||||
| Densidade da espinha dendrítica em o núcleo accumbens | ↓ | ↑ | ↑ | ||||
Dependência e abstinência
A tolerância às drogas se desenvolve rapidamente no abuso de anfetaminas (ou seja, uso recreativo de anfetaminas), portanto, períodos de abuso prolongado exigem doses cada vez maiores da droga para obter o mesmo efeito. De acordo com uma revisão da Cochrane sobre abstinência em indivíduos que usam compulsivamente anfetaminas e metanfetaminas, "quando usuários pesados crônicos descontinuam abruptamente o uso de anfetaminas, muitos relatam uma síndrome de abstinência por tempo limitado que ocorre dentro de 24 horas após a última dose".; Esta revisão observou que os sintomas de abstinência em usuários crônicos de altas doses são frequentes, ocorrendo em cerca de 88% dos casos e persistem por 3–4 semanas com uma marcada " falha" fase que ocorre durante a primeira semana. Os sintomas de abstinência de anfetaminas podem incluir ansiedade, desejo por drogas, humor deprimido, fadiga, aumento do apetite, aumento ou diminuição do movimento, falta de motivação, insônia ou sonolência e sonhos lúcidos. A revisão indicou que a gravidade dos sintomas de abstinência está positivamente correlacionada com a idade do indivíduo e a extensão de sua dependência. Sintomas leves de abstinência decorrentes da descontinuação do tratamento com anfetaminas em doses terapêuticas podem ser evitados diminuindo a dose.
Overdose
Uma overdose de anfetamina pode levar a muitos sintomas diferentes, mas raramente é fatal com os cuidados adequados. A gravidade dos sintomas de overdose aumenta com a dosagem e diminui com a tolerância à anfetamina. Sabe-se que indivíduos tolerantes tomam até 5 gramas de anfetamina por dia, o que é aproximadamente 100 vezes a dose terapêutica diária máxima. Os sintomas de uma overdose moderada e extremamente grande estão listados abaixo; envenenamento fatal por anfetamina geralmente também envolve convulsões e coma. Em 2013, overdose de anfetaminas, metanfetaminas e outros compostos implicados em um "distúrbio do uso de anfetaminas" resultou em cerca de 3.788 mortes em todo o mundo (3.425–4.145 mortes, 95% confiança).
| Sistema | Sobredosagem menor ou moderada | Sobredosagem grave |
|---|---|---|
| Cirurgia |
|
|
| Sistema nervoso central |
|
|
| Musculosqueleto |
|
|
| Respiração |
|
|
| Urinária |
|
|
| Outros |
|
|
Toxicidade
Em roedores e primatas, doses suficientemente altas de anfetamina causam neurotoxicidade dopaminérgica, ou dano aos neurônios dopaminérgicos, que é caracterizado por degeneração do terminal de dopamina e função reduzida do transportador e do receptor. Não há evidências de que a anfetamina seja diretamente neurotóxica em humanos. No entanto, grandes doses de anfetamina podem causar indiretamente neurotoxicidade dopaminérgica como resultado de hiperpirexia, formação excessiva de espécies reativas de oxigênio e aumento da auto-oxidação da dopamina. Modelos animais de neurotoxicidade da exposição a altas doses de anfetaminas indicam que a ocorrência de hiperpirexia (ou seja, temperatura corporal central ≥ 40 °C) é necessária para o desenvolvimento de neurotoxicidade induzida por anfetaminas. Elevações prolongadas da temperatura cerebral acima de 40 °C provavelmente promovem o desenvolvimento de neurotoxicidade induzida por anfetaminas em animais de laboratório, facilitando a produção de espécies reativas de oxigênio, interrompendo a função da proteína celular e aumentando transitoriamente a permeabilidade da barreira hematoencefálica.
Psicose
Uma overdose de anfetamina pode resultar em uma psicose estimulante que pode envolver uma variedade de sintomas, como delírios e paranóia. Uma revisão da Cochrane sobre tratamento para psicose por anfetamina, dextroanfetamina e metanfetamina afirma que cerca de 5–15% dos usuários não conseguem se recuperar completamente. De acordo com a mesma revisão, há pelo menos um estudo que mostra que os medicamentos antipsicóticos efetivamente resolvem os sintomas da psicose aguda causada por anfetaminas. A psicose raramente surge do uso terapêutico.
Interações medicamentosas
Sabe-se que muitos tipos de substâncias interagem com a anfetamina, resultando na alteração da ação da droga ou no metabolismo da anfetamina, da substância que interage ou de ambos. Os inibidores das enzimas que metabolizam a anfetamina (por exemplo, CYP2D6 e FMO3) prolongarão sua meia-vida de eliminação, o que significa que seus efeitos serão mais duradouros. A anfetamina também interage com os MAOIs, particularmente os inibidores da monoamina oxidase A, uma vez que tanto os IMAOs quanto a anfetamina aumentam as catecolaminas plasmáticas (ou seja, norepinefrina e dopamina); portanto, o uso simultâneo de ambos é perigoso. A anfetamina modula a atividade da maioria das drogas psicoativas. Em particular, as anfetaminas podem diminuir os efeitos de sedativos e depressores e aumentar os efeitos de estimulantes e antidepressivos. A anfetamina também pode diminuir os efeitos dos anti-hipertensivos e antipsicóticos devido aos seus efeitos sobre a pressão arterial e a dopamina, respectivamente. A suplementação de zinco pode reduzir a dose efetiva mínima de anfetamina quando usada no tratamento do TDAH.
Em geral, não há interação significativa ao consumir anfetaminas com alimentos, mas o pH do conteúdo gastrointestinal e da urina afeta a absorção e a excreção de anfetaminas, respectivamente. Substâncias ácidas reduzem a absorção de anfetaminas e aumentam a excreção urinária, e substâncias alcalinas fazem o oposto. Devido ao efeito do pH na absorção, a anfetamina também interage com redutores de ácido gástrico, como inibidores da bomba de prótons e anti-histamínicos H2, que aumentam o pH gastrointestinal (ou seja, o tornam menos ácido).
Farmacologia
Farmacodinâmica
Farmacodinâmica da anfetamina em um neurônio da dopamina |
A anfetamina exerce seus efeitos comportamentais alterando o uso de monoaminas como sinais neuronais no cérebro, principalmente em neurônios catecolamínicos nas vias de recompensa e função executiva do cérebro. As concentrações dos principais neurotransmissores envolvidos nos circuitos de recompensa e no funcionamento executivo, dopamina e norepinefrina, aumentam dramaticamente de maneira dose-dependente pela anfetamina por causa de seus efeitos nos transportadores de monoamina. Os efeitos reforçadores e promotores de saliência motivacional da anfetamina são devidos principalmente ao aumento da atividade dopaminérgica na via mesolímbica. Os efeitos eufóricos e estimulantes da locomoção da anfetamina dependem da magnitude e da velocidade com que ela aumenta as concentrações sinápticas de dopamina e norepinefrina no corpo estriado.
A anfetamina foi identificada como um potente agonista total do receptor 1 associado à amina (TAAR1), um Gs-acoplado e Gq- receptor acoplado à proteína G acoplado (GPCR) descoberto em 2001, o que é importante para a regulação das monoaminas cerebrais. A ativação do TAAR1 aumenta a produção de cAMP por meio da ativação da adenilil ciclase e inibe a função do transportador de monoamina. Autorreceptores de monoamina (por exemplo, D2 curto, α2 pré-sináptico e 5-HT1A pré-sináptico) têm o efeito oposto de TAAR1 e, juntos, esses receptores fornecem um sistema regulador para monoaminas. Notavelmente, as anfetaminas e as aminas traço possuem altas afinidades de ligação para TAAR1, mas não para autorreceptores de monoamina. Estudos de imagem indicam que a inibição da recaptação de monoamina por anfetaminas e aminas traço é específica do local e depende da presença de TAAR1 co-localização nos neurônios monoamina associados.
Além dos transportadores neuronais de monoamina, a anfetamina também inibe os transportadores vesiculares de monoamina, VMAT1 e VMAT2, bem como SLC1A1, SLC22A3 e SLC22A5. SLC1A1 é o transportador de aminoácidos excitatórios 3 (EAAT3), um transportador de glutamato localizado em neurônios, SLC22A3 é um transportador de monoamina extraneuronal que está presente em astrócitos e SLC22A5 é um transportador de carnitina de alta afinidade. A anfetamina é conhecida por induzir fortemente a expressão do gene transcrito regulado por cocaína e anfetamina (CART), um neuropeptídeo envolvido no comportamento alimentar, estresse e recompensa, que induz aumentos observáveis no desenvolvimento neuronal e na sobrevivência in vitro. O receptor CART ainda não foi identificado, mas há evidências significativas de que o CART se liga a um único Gi/Go-coupled GPCR . A anfetamina também inibe as monoamina oxidases em doses muito altas, resultando em menor metabolismo de monoaminas e aminas residuais e, conseqüentemente, em concentrações mais altas de monoaminas sinápticas. Em humanos, o único receptor pós-sináptico ao qual se sabe que a anfetamina se liga é o receptor 5-HT1A, onde atua como um agonista com baixa afinidade micromolar.
O perfil completo dos efeitos de drogas de curto prazo da anfetamina em humanos é derivado principalmente através do aumento da comunicação celular ou neurotransmissão de dopamina, serotonina, norepinefrina, epinefrina, histamina, peptídeos CART, opióides endógenos, hormônio adrenocorticotrófico, corticosteróides, e glutamato, que afeta através de interações com CART, 5-HT1A , EAAT3, TAAR1, VMAT1, VMAT2 e possivelmente outros alvos biológicos. A anfetamina também ativa sete enzimas da anidrase carbônica humana, várias das quais são expressas no cérebro humano.
A dextroanfetamina é um agonista mais potente do TAAR1 do que a levoanfetamina. Consequentemente, a dextroanfetamina produz maior estimulação do SNC do que a levoanfetamina, cerca de três a quatro vezes mais, mas a levoanfetamina tem efeitos cardiovasculares e periféricos ligeiramente mais fortes.
Dopamina
Em certas regiões do cérebro, a anfetamina aumenta a concentração de dopamina na fenda sináptica. A anfetamina pode entrar no neurônio pré-sináptico através do DAT ou difundindo-se diretamente através da membrana neuronal. Como consequência da captação de DAT, a anfetamina produz inibição competitiva da recaptação no transportador. Ao entrar no neurônio pré-sináptico, a anfetamina ativa o TAAR1 que, por meio da sinalização da proteína quinase A (PKA) e da proteína quinase C (PKC), causa a fosforilação do DAT. A fosforilação por qualquer proteína quinase pode resultar na internalização de DAT (inibição não competitiva da recaptação), mas a fosforilação mediada por PKC sozinha induz a reversão do transporte de dopamina através do DAT (ou seja, efluxo de dopamina). A anfetamina também é conhecida por aumentar o cálcio intracelular, um efeito que está associado à fosforilação de DAT por meio de uma via não identificada de proteína quinase dependente de Ca2+/calmodulina (CAMK), que, por sua vez, produz efluxo de dopamina. Por meio da ativação direta de canais de potássio de retificação interna acoplados à proteína G, o TAAR1 reduz a taxa de disparo dos neurônios dopaminérgicos, evitando um estado hiperdopaminérgico.
A anfetamina também é um substrato para o transportador de monoamina vesicular pré-sináptica, VMAT2. Após a captação de anfetamina no VMAT2, a anfetamina induz o colapso do gradiente de pH vesicular, o que resulta na liberação de moléculas de dopamina das vesículas sinápticas para o citosol via efluxo de dopamina através do VMAT2. Subsequentemente, as moléculas citosólicas de dopamina são liberadas do neurônio pré-sináptico para a fenda sináptica via transporte reverso no DAT.
Norepinefrina
Semelhante à dopamina, a anfetamina aumenta dose-dependente o nível de norepinefrina sináptica, o precursor direto da epinefrina. Com base na expressão de TAAR1 mRNA neuronal, acredita-se que a anfetamina afete a norepinefrina de forma análoga à dopamina. Em outras palavras, a anfetamina induz o efluxo mediado por TAAR1 e inibição da recaptação não competitiva no NET fosforilado, inibição competitiva da recaptação do NET, e liberação de norepinefrina do VMAT2.
Serotonina
A anfetamina exerce efeitos análogos, porém menos pronunciados, na serotonina quanto na dopamina e norepinefrina. A anfetamina afeta a serotonina por meio do VMAT2 e, como a norepinefrina, fosforila o SERT por meio de TAAR1. Como a dopamina, a anfetamina tem baixa afinidade micromolar no receptor 5-HT1A humano.
Outros neurotransmissores, peptídeos, hormônios e enzimas
| Enzima | KKA (nM) | Fontes |
|---|---|---|
| HCA4 | 94 | |
| HCA5A | 810 | |
| HCA5B | 2560 | |
| HCA7 | 910 | |
| HCA12 | 640 | |
| HCA13 | 24100 | |
| HCA14 | 9150 |
A administração aguda de anfetaminas em humanos aumenta a liberação endógena de opioides em várias estruturas cerebrais no sistema de recompensa. Os níveis extracelulares de glutamato, o principal neurotransmissor excitatório no cérebro, demonstraram aumentar no corpo estriado após a exposição à anfetamina. Este aumento no glutamato extracelular provavelmente ocorre através da internalização induzida por anfetaminas de EAAT3, um transportador de recaptação de glutamato, em neurônios dopaminérgicos. A anfetamina também induz a liberação seletiva de histamina de mastócitos e efluxo de neurônios histaminérgicos através do VMAT2. A administração aguda de anfetaminas também pode aumentar os níveis de hormônio adrenocorticotrófico e corticosteróides no plasma sanguíneo, estimulando o eixo hipotálamo-hipófise-adrenal.
Em dezembro de 2017, foi publicado o primeiro estudo avaliando a interação entre a anfetamina e as enzimas da anidrase carbônica humana; das onze enzimas da anidrase carbônica examinadas, descobriu-se que a anfetamina ativa potentemente sete, quatro das quais são altamente expressas no cérebro humano, com efeitos de ativação de baixo nanomolar a baixo micromolar. Com base em pesquisas pré-clínicas, a ativação da anidrase carbônica cerebral tem efeitos de aprimoramento da cognição; mas, com base no uso clínico de inibidores da anidrase carbônica, a ativação da anidrase carbônica em outros tecidos pode estar associada a efeitos adversos, como ativação ocular exacerbando o glaucoma.
Farmacocinética
A biodisponibilidade oral da anfetamina varia com o pH gastrointestinal; é bem absorvido pelo intestino e a biodisponibilidade é tipicamente superior a 75% para a dextroanfetamina. A anfetamina é uma base fraca com um pKa de 9,9; conseqüentemente, quando o pH é básico, mais fármaco está em sua forma de base livre solúvel em lipídios e mais é absorvido pelas membranas celulares ricas em lipídeos do epitélio intestinal. Por outro lado, um pH ácido significa que o fármaco está predominantemente na forma catiônica (sal) solúvel em água e menos é absorvido. Aproximadamente 20% da anfetamina circulante na corrente sanguínea está ligada às proteínas plasmáticas. Após a absorção, a anfetamina se distribui prontamente na maioria dos tecidos do corpo, com altas concentrações ocorrendo no líquido cefalorraquidiano e no tecido cerebral.
As meias-vidas dos enantiômeros das anfetaminas diferem e variam com o pH da urina. Em pH urinário normal, as meias-vidas da dextroanfetamina e da levoanfetamina são 9–11 horas e 11–14 horas, respectivamente. A urina altamente ácida reduzirá as meias-vidas dos enantiômeros para 7 horas; urina altamente alcalina aumentará as meias-vidas em até 34 horas. As variantes de liberação imediata e liberação prolongada de sais de ambos os isômeros atingem concentrações plasmáticas máximas em 3 horas e 7 horas após a dose, respectivamente. A anfetamina é eliminada pelos rins, com 30–40% da droga sendo excretada inalterada em pH urinário normal. Quando o pH urinário é básico, a anfetamina está em sua forma de base livre, então menos é excretada. Quando o pH da urina é anormal, a recuperação urinária da anfetamina pode variar de um mínimo de 1% a um máximo de 75%, dependendo principalmente se a urina é muito básica ou ácida, respectivamente. Após a administração oral, a anfetamina aparece na urina dentro de 3 horas. Aproximadamente 90% da anfetamina ingerida é eliminada 3 dias após a última dose oral.
A lisdexanfetamina é um pró-fármaco da dextroanfetamina. Não é tão sensível ao pH quanto a anfetamina ao ser absorvida no trato gastrointestinal. Após a absorção na corrente sanguínea, a lisdexanfetamina é completamente convertida pelos glóbulos vermelhos em dextroanfetamina e no aminoácido L-lisina por hidrólise através de enzimas aminopeptidases indeterminadas. Esta é a etapa limitante da taxa na bioativação da lisdexanfetamina. A meia-vida de eliminação da lisdexanfetamina é geralmente inferior a 1 hora. Devido à conversão necessária de lisdexanfetamina em dextroanfetamina, os níveis de dextroanfetamina com lisdexanfetamina atingem o pico cerca de uma hora mais tarde do que com uma dose equivalente de dextroanfetamina de libertação imediata. Presumivelmente devido à sua taxa de ativação limitada pelos glóbulos vermelhos, a administração intravenosa de lisdexanfetamina mostra um tempo de pico muito atrasado e níveis de pico reduzidos em comparação com a administração intravenosa de uma dose equivalente de dextroanfetamina. A farmacocinética da lisdexanfetamina é semelhante, independentemente de ser administrada por via oral, intranasal ou intravenosa. Assim, em contraste com a dextroanfetamina, o uso parenteral não aumenta os efeitos subjetivos da lisdexanfetamina. Devido ao seu comportamento como pró-fármaco e às suas diferenças farmacocinéticas, a lisdexanfetamina tem uma duração mais longa do efeito terapêutico do que a dextroanfetamina de libertação imediata e apresenta um potencial de utilização indevida reduzido.
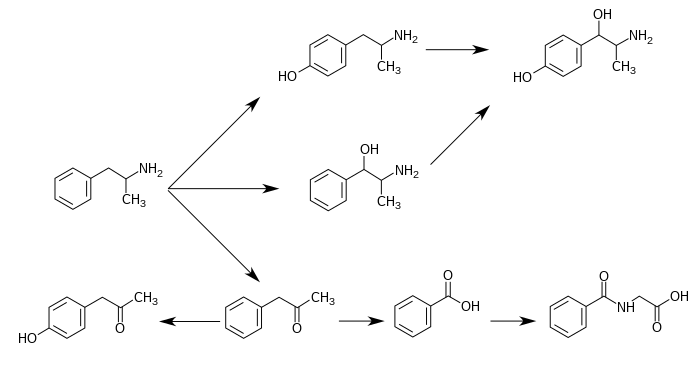
CYP2D6, dopamina β-hidroxilase (DBH), monooxigenase 3 contendo flavina (FMO3), butirato-CoA ligase (XM-ligase) e glicina N-aciltransferase (GLYAT) são as enzimas conhecidas por metabolizar a anfetamina ou seus metabólitos em humanos. A anfetamina tem uma variedade de produtos metabólicos excretados, incluindo 4-hidroxianfetamina, 4-hidroxinorefedrina, 4-hidroxifenilacetona, ácido benzóico, ácido hipúrico, norefedrina e fenilacetona. Entre esses metabólitos, os simpatomiméticos ativos são 4-hidroxianfetamina, 4-hidroxinorefedrina e norefedrina. As principais vias metabólicas envolvem para-hidroxilação aromática, alfa- e beta-hidroxilação alifática, N-oxidação, N-desalquilação e desaminação. As vias metabólicas conhecidas, metabólitos detectáveis e enzimas metabolizadoras em humanos incluem o seguinte:
Caminhos metabólicos da anfetamina em humanos |
Farmacomicrobiômica
O metagenoma humano (ou seja, a composição genética de um indivíduo e todos os microorganismos que residem no corpo do indivíduo ou dentro dele) varia consideravelmente entre os indivíduos. Como o número total de células microbianas e virais no corpo humano (mais de 100 trilhões) supera em muito o número de células humanas (dezenas de trilhões), existe um potencial considerável para interações entre medicamentos e o microbioma de um indivíduo, incluindo: medicamentos que alteram o composição do microbioma humano, metabolismo de drogas por enzimas microbianas modificando o perfil farmacocinético da droga e metabolismo de drogas microbianas afetando a eficácia clínica e o perfil de toxicidade de uma droga. O campo que estuda essas interações é conhecido como farmacomicrobiômica.
Semelhante à maioria das biomoléculas e outros xenobióticos administrados por via oral (ou seja, drogas), prevê-se que a anfetamina sofra metabolismo promíscuo pela microbiota gastrointestinal humana (principalmente bactérias) antes da absorção na corrente sanguínea. A primeira enzima microbiana metabolizadora de anfetaminas, a tiramina oxidase de uma cepa de E. coli comumente encontrada no intestino humano, foi identificada em 2019. Verificou-se que essa enzima metaboliza anfetamina, tiramina e fenetilamina com aproximadamente a mesma afinidade de ligação para todos os três compostos.
Compostos endógenos relacionados
A anfetamina tem estrutura e função muito semelhantes às aminas endógenas, que são moléculas neuromoduladoras de ocorrência natural produzidas no corpo e no cérebro humanos. Entre este grupo, os compostos mais estreitamente relacionados são fenetilamina, o composto original da anfetamina, e N-metilfenetilamina, um isômero da anfetamina (ou seja, tem uma fórmula molecular idêntica). Em humanos, a fenetilamina é produzida diretamente da L-fenilalanina pela enzima aminoácido aromático descarboxilase (AADC), que converte a L-DOPA em dopamina também. Por sua vez, a N-metilfenetilamina é metabolizada da fenetilamina pela feniletanolamina N-metiltransferase, a mesma enzima que metaboliza a norepinefrina em epinefrina. Como a anfetamina, tanto a fenetilamina quanto a N-metilfenetilamina regulam a neurotransmissão da monoamina via TAAR1; ao contrário da anfetamina, ambas as substâncias são decompostas pela monoamina oxidase B e, portanto, têm uma meia-vida mais curta do que a anfetamina.
Química
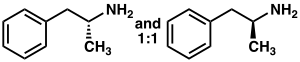
Amfetaminas de raça |
A anfetamina é um homólogo metil do neurotransmissor fenetilamina de mamíferos com a fórmula química C9H13N. O átomo de carbono adjacente à amina primária é um centro estereogênico, e a anfetamina é composta por uma mistura racêmica 1:1 de dois enantiômeros. Essa mistura racêmica pode ser separada em seus isômeros ópticos: levoanfetamina e dextroanfetamina. À temperatura ambiente, a base livre pura da anfetamina é um líquido móvel, incolor e volátil com um forte odor característico de amina e um sabor acre e ardente. Os sais sólidos de anfetamina frequentemente preparados incluem adipato, aspartato, cloridrato, fosfato, sacarato, sulfato e tanato de anfetamina. O sulfato de dextroanfetamina é o sal enantiopuro mais comum. A anfetamina também é o composto parental de sua própria classe estrutural, que inclui vários derivados psicoativos. Em química orgânica, a anfetamina é um excelente ligante quiral para a síntese estereosseletiva de 1,1'-bi-2-naftol.
Derivados substituídos
Os derivados substituídos da anfetamina, ou "anfetaminas substituídas", são uma ampla gama de produtos químicos que contêm anfetamina como uma "espinha dorsal"; especificamente, esta classe química inclui compostos derivados que são formados pela substituição de um ou mais átomos de hidrogênio na estrutura central da anfetamina por substituintes. A classe inclui a própria anfetamina, estimulantes como a metanfetamina, empatógenos serotoninérgicos como o MDMA e descongestionantes como a efedrina, entre outros subgrupos.
Síntese
Desde que a primeira preparação foi relatada em 1887, várias rotas sintéticas para a anfetamina foram desenvolvidas. A rota mais comum de síntese de anfetaminas legais e ilícitas emprega uma redução não metálica conhecida como reação de Leuckart (método 1). Na primeira etapa, uma reação entre fenilacetona e formamida, usando ácido fórmico adicional ou a própria formamida como agente redutor, produz N-formilanfetamina. Este intermediário é então hidrolisado com ácido clorídrico e posteriormente basificado, extraído com solvente orgânico, concentrado e destilado para produzir a base livre. A base livre é então dissolvida em um solvente orgânico, ácido sulfúrico é adicionado e a anfetamina precipita como o sal sulfato.
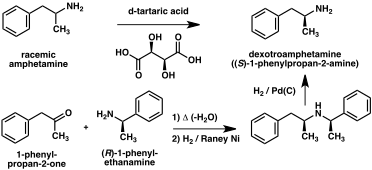
Várias resoluções quirais foram desenvolvidas para separar os dois enantiômeros da anfetamina. Por exemplo, a anfetamina racêmica pode ser tratada com ácido d-tartárico para formar um sal diastereoisomérico que é cristalizado fracionadamente para produzir dextroanfetamina. A resolução quiral continua sendo o método mais econômico para obtenção de anfetamina opticamente pura em grande escala. Além disso, várias sínteses enantiosseletivas de anfetaminas foram desenvolvidas. Em um exemplo, (R)-1-fenil-etanamina opticamente puro é condensado com fenilacetona para produzir uma base de Schiff quiral. Na etapa chave, esse intermediário é reduzido por hidrogenação catalítica com transferência de quiralidade para o átomo de carbono alfa para o grupo amino. A clivagem da ligação amina benzílica por hidrogenação produz dextroanfetamina opticamente pura.
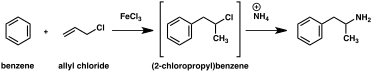
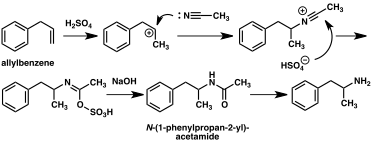
Um grande número de rotas sintéticas alternativas à anfetamina foi desenvolvido com base em reações orgânicas clássicas. Um exemplo é a alquilação de Friedel-Crafts de benzeno por cloreto de alila para produzir beta cloropropilbenzeno que é então reagido com amônia para produzir anfetamina racêmica (método 2). Outro exemplo emprega a reação de Ritter (método 3). Nesta rota, o alilbenzeno é feito reagir com acetonitrila em ácido sulfúrico para produzir um organossulfato que por sua vez é tratado com hidróxido de sódio para dar anfetamina através de um intermediário acetamida. Uma terceira rota começa com 3-oxobutanoato de etil que através de uma dupla alquilação com iodeto de metila seguido de cloreto de benzila pode ser convertido em 2-metil-3 ácido -fenil-propanóico. Este intermediário sintético pode ser transformado em anfetamina usando um rearranjo de Hofmann ou Curtius (método 4).
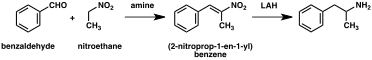
Um número significativo de sínteses de anfetaminas apresenta uma redução de nitro, imina, oxima ou outros grupos funcionais contendo nitrogênio. Em um desses exemplos, uma condensação Knoevenagel de benzaldeído com nitroetano produz fenil-2-nitropropeno. A ligação dupla e o grupo nitro deste intermediário são reduzidos usando hidrogenação catalítica ou por tratamento com hidreto de alumínio e lítio (método 5). Outro método é a reação da fenilacetona com amônia, produzindo uma imina intermediária que é reduzida à amina primária usando hidrogênio sobre um catalisador de paládio ou hidreto de alumínio e lítio (método 6).
Detecção em fluidos corporais
A anfetamina é frequentemente medida na urina ou no sangue como parte de um teste de drogas para esportes, emprego, diagnóstico de envenenamento e forense. Técnicas como o imunoensaio, que é a forma mais comum de teste de anfetamina, podem apresentar reação cruzada com vários medicamentos simpatomiméticos. Métodos cromatográficos específicos para anfetaminas são empregados para prevenir resultados falso-positivos. Técnicas de separação quiral podem ser empregadas para ajudar a distinguir a fonte da droga, seja anfetamina prescrita, pró-drogas de anfetamina prescritas (por exemplo, selegilina), medicamentos de venda livre que contenham levometanfetamina ou anfetaminas substituídas obtidas ilicitamente. Vários medicamentos prescritos produzem anfetamina como metabólito, incluindo benzfetamina, clobenzorex, famprofazona, fenproporex, lisdexanfetamina, mesocarbe, metanfetamina, prenilamina e selegilina, entre outros. Esses compostos podem produzir resultados positivos para anfetaminas em testes de drogas. A anfetamina geralmente só é detectável por um teste de drogas padrão por aproximadamente 24 horas, embora uma dose alta possa ser detectada por 2–4 dias.
Para os ensaios, um estudo observou que um ensaio de técnica de imunoensaio de enzima multiplicada (EMIT) para anfetamina e metanfetamina pode produzir mais falsos positivos do que cromatografia líquida-espectrometria de massa em tandem. Cromatografia gasosa-espectrometria de massa (GC-MS) de anfetamina e metanfetamina com o agente derivatizante cloreto (S)-(−)-trifluoroacetilprolil permite a detecção de metanfetamina na urina. A GC-MS de anfetamina e metanfetamina com o agente derivatizante quiral cloreto de ácido de Mosher permite a detecção de dextroanfetamina e dextrometanfetamina na urina. Portanto, o último método pode ser usado em amostras com teste positivo usando outros métodos para ajudar a distinguir entre as várias fontes da droga.
História, sociedade e cultura
| Substância | Melhor estimativa | Baixa estimativa | Alto. estimativa |
|---|---|---|---|
| Estimulantes do tipo anfetamina | 34.16 | 13.42 | 55.24 |
| Cannabis | 192.15 | 165.76 | 234.06 |
| Cocaína | 18.20 | 13.87 | 22.85 |
| Ecstasy | 20.57 | 8.99 | 32.34 |
| Opiáceos | 19.38 | 13.80 | 26.15 |
| Opiáceos | 34.26 | 27.01 | 44.54 |
Estimulantes do tipo anfetamina foram originalmente derivados da planta Efedrina, que contém o estimulante semelhante à anfetamina efedrina e foi usado por seus efeitos na China desde cerca de 5.000 anos. A efedrina foi isolada da Ephedra vulgaris no Japão em 1885 e foi estudada por suas propriedades medicinais na década de 1920. As escassas quantidades de efedrina na planta Efedrina levaram a investigações de análogos sintéticos da efedrina.
A anfetamina foi sintetizada pela primeira vez em 1887 na Alemanha pelo químico romeno Lazăr Edeleanu, que a chamou de fenilisopropilamina; seus efeitos estimulantes permaneceram desconhecidos até 1927, quando foi ressintetizado independentemente por Gordon Alles e relatado como tendo propriedades simpatomiméticas. A anfetamina não teve uso médico até o final de 1933, quando Smith, Kline e French começaram a vendê-la como um inalador sob a marca Benzedrine como descongestionante. O sulfato de benzedrina foi introduzido 3 anos depois e era usado para tratar uma ampla variedade de condições médicas, incluindo narcolepsia, obesidade, pressão arterial baixa, baixa libido e dor crônica, entre outras. O efeito benéfico da benzedrina em crianças com hiperatividade foi descoberto por acaso em 1937, quando foi administrado contra uma cefaleia de baixa pressão intracraniana. Não melhorou a dor de cabeça, mas melhorou o desempenho escolar e o comportamento de alguns. Durante a Segunda Guerra Mundial, a anfetamina e a metanfetamina foram usadas extensivamente pelas forças aliadas e do Eixo por seus efeitos estimulantes e de melhoria de desempenho. À medida que as propriedades viciantes da droga se tornaram conhecidas, os governos começaram a impor controles rígidos sobre a venda de anfetaminas. Por exemplo, durante o início da década de 1970 nos Estados Unidos, a anfetamina tornou-se uma substância controlada do cronograma II de acordo com a Lei de Substâncias Controladas. Apesar dos rígidos controles governamentais, a anfetamina tem sido usada legal ou ilicitamente por pessoas de diversas origens, incluindo autores, músicos, matemáticos e atletas.
A anfetamina ainda hoje é sintetizada ilegalmente em laboratórios clandestinos e vendida no mercado negro, principalmente em países europeus. Entre os estados membros da União Europeia (UE) em 2018, 11,9 milhões de adultos de idades 15–64 usaram anfetaminas ou metanfetaminas pelo menos uma vez na vida e 1,7 milhões usaram no ano passado. Durante 2012, aproximadamente 5,9 toneladas métricas de anfetaminas ilícitas foram apreendidas nos estados membros da UE; o "preço de rua" de anfetamina ilícita na UE variou de € 6–38 por grama durante o mesmo período. Fora da Europa, o mercado ilícito de anfetaminas é muito menor do que o mercado de metanfetaminas e MDMA.
Estatuto legal
Como resultado da Convenção das Nações Unidas sobre Substâncias Psicotrópicas de 1971, a anfetamina tornou-se uma substância controlada da tabela II, conforme definido no tratado, em todos os 183 estados participantes. Consequentemente, é fortemente regulamentado na maioria dos países. Alguns países, como a Coréia do Sul e o Japão, proibiram as anfetaminas substitutas, mesmo para uso médico. Em outras nações, como Canadá (drogas da lista I), Holanda (drogas da Lista I), Estados Unidos (drogas da lista II), Austrália (drogas da lista 8), Tailândia (narcóticos da categoria 1) e Reino Unido (drogas da classe B), a anfetamina está em uma tabela nacional restritiva de drogas que permite seu uso como tratamento médico.
Produtos farmacêuticos
Várias formulações de anfetaminas atualmente comercializadas contêm ambos os enantiômeros, incluindo aquelas comercializadas sob as marcas Adderall, Adderall XR, Mydayis, Adzenys ER, Adzenys XR-ODT, Dyanavel XR, Evekeo e Evekeo ODT. Desses, Evekeo (incluindo Evekeo ODT) é o único produto que contém apenas anfetamina racêmica (como sulfato de anfetamina) e, portanto, é o único cuja porção ativa pode ser referida com precisão simplesmente como "anfetamina". A dextroanfetamina, comercializada sob as marcas Dexedrine e Zenzedi, é o único produto de anfetamina enantiopura disponível atualmente. Uma forma pró-droga de dextroanfetamina, lisdexanfetamina, também está disponível e é comercializada sob a marca Vyvanse. Por ser um pró-fármaco, a lisdexanfetamina é estruturalmente diferente da dextroanfetamina, sendo inativa até ser metabolizada em dextroanfetamina. A base livre da anfetamina racêmica estava anteriormente disponível como Benzedrine, Psychedrine e Sympatedrine. A levoanfetamina estava anteriormente disponível como Cydril. Muitos produtos farmacêuticos de anfetaminas atuais são sais devido à volatilidade comparativamente alta da base livre. No entanto, as formas farmacêuticas de suspensão oral e comprimido de desintegração oral (ODT) compostas pela base livre foram introduzidas em 2015 e 2016, respectivamente. Algumas das marcas atuais e seus equivalentes genéricos estão listados abaixo.
| Marca Nome | Estados Unidos Nome adotado | (D:L) relação | Dosagem formulário | Marketing data de início | Consumidores americanos dados de preço | Fontes |
|---|---|---|---|---|---|---|
| Adderall | – | 3:1(saltes) | tablet | 1996 | Bom dia. | |
| Adicionar ao cesto | – | 3:1(saltes) | cápsula | 2001 | Bom dia. | |
| O meu dia | – | 3:1(saltes) | cápsula | 2017 | Bom dia. | |
| Adzenys ER | anfetamina | 3:1(base) | suspensão | 2017 | Bom dia. | |
| Adzenys XR-ODT | anfetamina | 3:1(base) | ODT | 2016 | Bom dia. | |
| Dyanavel XR | anfetamina | 3.2:1(base) | suspensão | 2015 | Bom dia. | |
| Evekeo | sulfato de anfetamina | 1:1(saltes) | tablet | 2012 | Bom dia. | |
| O que fazer? | sulfato de anfetamina | 1:1(saltes) | ODT | 2019 | Bom dia. | |
| Dexedrina | dextroamphetamine sulfato | 1:0(saltes) | cápsula | 1976 | Bom dia. | |
| Zenzedi | dextroamphetamine sulfato | 1:0(saltes) | tablet | 2013 | Bom dia. | |
| Vyvans | lisdexamfetamine dimesylate | 1:0(prodrug) | cápsula | 2007 | Bom dia. | |
| tablet | ||||||
| Xelstrym | Dextroamphetamina | 1:0(base) | patch | 2022 | Bom dia. |
| droga | fórmula | massa molar | base de anfetamina | base de anfetamina em doses iguais | doses com Base igual conteúdo | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| (g/mol) | (porcento) | (30 mg de dose) | ||||||||
| total | base | total | Dextro... | levo... | Dextro... | levo... | ||||
| dextroamphetamine sulfato | (C)9H. H. H.13N)2• H. H. H.2Então...4 | 368.49 | 270.41 | 73,38% | 73,38% | — | 22.0 mg | — | 30,0 mg | |
| sulfato de anfetamina | (C)9H. H. H.13N)2• H. H. H.2Então...4 | 368.49 | 270.41 | 73,38% | 36,69% | 36,69% | 11,0 mg | 11,0 mg | 30,0 mg | |
| Adderall | 6,57% | 47,49% | 15.08% | 14,2 mg | 4.5 mg | 35,2 mg | ||||
| 25% | dextroamphetamine sulfato | (C)9H. H. H.13N)2• H. H. H.2Então...4 | 368.49 | 270.41 | 73,38% | 73,38% | — | |||
| 25% | sulfato de anfetamina | (C)9H. H. H.13N)2• H. H. H.2Então...4 | 368.49 | 270.41 | 73,38% | 36,69% | 36,69% | |||
| 25% | Dextroamphetamine saccharate | (C)9H. H. H.13N)2•C6H. H. H.10.O8 | 48,5 | 270.41 | 56.27% | 56.27% | — | |||
| 25% | monohidrato de aspartato de amfetamina | (C)9H. H. H.13N)•C4H. H. H.7Não.4• H. H. H.2O | 286.32 | 135.21 | 47,22% | 23,61% | 23,61% | |||
| lisdexamfetamine dimesylate | C15H. H. H.25N3O• (CH)4O3S)2 | 455.49 | 135.21 | 29,68% | 29,68% | — | 8.9 mg | — | 74.2 mg | |
| suspensão da base da anfetamina | C9H. H. H.13N | 135.21 | 135.21 | 100% | 76.19% | 23,81% | 22,9 mg | 7.1 mg | 22.0 mg | |
Notas de referência
- ^
- ^
- ^
- ^
- ^
- ^
- ^
- ^
- ↑ a b
- ^
- ^
- ^
- ^
- ↑ a b
- ^
- ↑ a b
- ^
Contenido relacionado
Frutarianismo
Amida
Grupo hidroxi