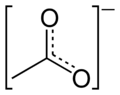
Acetato
um acetato é um sal formado pela combinação de ácido acético com uma base (por exemplo, alcalina, terrosa, metálica, não metálica ou base radical). " acetato " Descreve também a base ou íon conjugado (especificamente, o íon carregado negativamente chamado ânion) normalmente encontrado em solução aquosa e escrito com a fórmula química c
2
.
A maioria dos aproximadamente 5 milhões de toneladas de ácido acético produzido anualmente na indústria é usado na produção de acetatos, que geralmente assumem a forma de polímeros. Na natureza, o acetato é o bloco de construção mais comum para a biossíntese.
Nomenclatura e fórmula comum
Quando parte de um sal, a fórmula do íon acetato é escrita como ch
2 h
3 o -
. Os químicos geralmente representam acetato como OAC
Embora seu nome sistemático seja etanoato (), o acetato comum continua sendo o nome preferido da IUPAC.
Sals

O ânion acetato, [CH 3 COO]
- CH3O que fazer?3COO- Sim. + H+
Muitos sais de acetato são iônicos, indicados por sua tendência a se dissolver bem na água. Um acetato comumente encontrado na casa é o acetato de sódio, um sólido branco que pode ser preparado combinando vinagre e bicarbonato de sódio (" bicarbonato de refrigerante "):
- CH3COOH + NaHCO3 → CH3COO- Sim.Nao+ + H2O + CO2
metais de transição podem ser complexados por acetato. Exemplos de complexos de acetato incluem acetato de cromo (II) e acetato básico de zinco.
Os sais de acetato comercialmente importantes são acetato de alumínio, usado no tingimento, acetato de amônio, precursor da acetamida e acetato de potássio, usado como diurético. Todos os três sais são incolores e altamente solúveis em água.
Esters
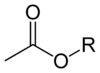
Quase metade da produção de ácido acético é consumido na produção de acetato de vinil, precursor do álcool polivinílico, que é um componente de muitas tintas. O segundo maior uso do ácido acético é consumido na produção de acetato de celulose. De fato, " Acetato " O jargão é o acetato de celulose, que é usado na produção de fibras ou produtos diversos, p. Os discos de acetato usados na produção de registros de áudio. O acetato de celulose pode ser encontrado em muitos produtos domésticos. Muitos solventes industriais são acetatos, incluindo acetato de metila, acetato de etila, acetato de isopropil, acetato de etilhexil. O acetato de butil é uma fragrância usada em produtos alimentícios.
Acetato em biologia
O acetato é um ânion comum em biologia. É utilizado principalmente por organismos na forma de acetil coenzima A.
A injeção intraperitoneal de acetato de sódio (20 ou 60 mg por kg de massa corporal) foi encontrada para induzir dor de cabeça em ratos sensibilizados, e foi proposto que o acetato resultante da oxidação do etanol é um fator importante na causa da ressaca. Os níveis aumentados de acetato sérico levam ao acúmulo de adenosina em muitos tecidos, incluindo o cérebro, e a administração do antagonista do receptor de adenosina cafeína a ratos após o etanol diminuiu o comportamento nociceptivo.O acetato conhece propriedades imunomoduladoras e pode afetar a resposta imune inata a bactérias patogênicas, como o patógeno respiratório haemophilus influenzae .
Acetil de fermentação CoA para acetato
O piruvato é convertido em acetil-coenzima A (acetil-CoA) pela enzima piruvato desidrogenase. Este acetil-CoA é então convertido em acetato em e. coli , enquanto produz ATP por fosforilação no nível do substrato. A formação de acetato requer duas enzimas: fosfato acetiltransferase e acetato quinase.

acetil-coa + fosfato → acetilfosfato + COA
acetil-fosfato + ADP → acetato + ATP
Fermentação de acetato
O ácido acético também pode sofrer uma reação de desmatutação para produzir metano e dióxido de carbono:
- CH3COO- Sim. + H+ → CH4 + CO2 ?G° = −36 kJ/mol
Esta reação de desproporção é catalisada por archaea de metanogênio em seu metabolismo fermentativo. Um elétron é transferido da função carbonil (doadora E - do grupo carboxílico para o grupo metil (aceitador E) do ácido acético, para produzir respectivamente CO
Estruturas
- Modelo de enchimento de espaço do anionato de acetato
- ressonância híbrida do âion acetato
- formas canônicas do anionato acetato
Ver também
- Acetilização
- Acetato de celulose
- Acetato de cobre (II)
- Fermentação (bioquímica)
- Acetato de sódio
- Fermentação de ácido misto
- Ácido acético
- Cloreto de acetilo
- Acetato de zinco
Referências
- ↑ a b Zumdahl, S. S. “Chemistry” Heath, 1986: Lexington, MA. ISBN 0-669-04529-2.
- ^ União Internacional de Química Pura e Aplicada (2005). Nomenclatura de Inorgânico Química (IUPAC Recomendações 2005). Cambridge (UK): RSC–IUPAC. ISBN 0-85404-438-8. p. 63. Versão electrónica.
- ^ Brimble, Margaret A.; Black, David StC.; Hartshorn, Richard; Rauter, Amélia P.; Sha, Chin-Kang; Sydnes, Leiv K. (10 novembro 2012). «Rules for abbreviation of protect groups (IUPAC Technical Report)» (em inglês). Química pura e aplicada. 85 (1): 310.10.1351/PAC-REP-12-07-12. S2CID 55102299.
- ^ R-9.1 Nomes triviais e semissistemamáticos retidos para nomear compostos orgânicos Arquivados 2014-02-08 na Wayback Machine, Guia de Nomenclatura IUPAC de Compostos Orgânicos, Comissão IUPAC sobre Nomenclatura da Química Orgânica
- ↑ a b Hosea Cheung, Robin S. Tanke, G. Paul Torrence "ácido acético" em Enciclopédia de Química Industrial de Ullmann Weinheim, Alemanha: Wiley-VCH, 2005. doi:10.1002/14356007.a01_045
- ^ Nelson, D. L.; Cox, M. M. "Lehninger, Principles of Biochemistry" 3rd Ed. Worth Publishing: New York, 2000. ISBN 1-57259-153-6.
- ^ Maxwell, Christina; et al. (2010). «Acetate Causes Alcohol Hangover Headache in Rats» (em inglês). PLOS UM. 5 (12): e15963. Código de acesso: 2010PLoSO...515963M. doi:10.1371/journal.pone.0015963. PMC 3013144. PMID 21209842.
- ^ 'É café a verdadeira cura para uma ressaca?' por Bob Holmes, New Scientist, 15 de janeiro de 2011, p. 17.
- ^ Hosmer, Jennifer; Nasreen, Marufa; Dhouib, Rabeb; Essilfie, Ama-Tawiah; Schirra, Horst Joachim; Henningham, Anna; Fantino, Emmanuelle; Sly, Peter; McEwan, Alastair G.; Kappler, Ulrike (2022-01-27). "Acesso a substratos de crescimento altamente especializados e produção de metabolitos imunomodulatórios epiteliais determinam a sobrevivência de Haemófilos influenzae em células epiteliais da via aérea humana". PLOS Patogens. 18. (1): e1010209. - Sim.10.1371/journal.ppat.1010209ISSN 1553-7374. PMC 8794153. PMID 35085362.
- ^ Keseler, Ingrid M.; et al. (2011). «EcoCyc: a abrangente database of Escherichia coli biologia». Pesquisa de Ácidos Nucleicos. 39 (Database issue): D583–D590. doi:10.1093/nar/gkq1143. PMC 3013716. PMID 21097882.
- ^ Ferry, J.G. (1992). "Metano do acetato". Journal of Bacteriology. 174 (17): 5489–5495. doi:10.1128/jb.174.17.5489-5495.1992. PMC 206491. PMID 1512186.
- ^ Vogels, G. D.; Keltjens, J. T.; Van Der Drift, C. (1988). «Biochemistry of methane production» (em inglês). Em Zehnder A.J.B. (ed.). Biologia de microrganismos anaeróbicos. Nova Iorque: Wiley. pp. 707–770.